El modelo
atómico de Rutherford es un modelo atómico o teoría sobre la estructura interna
del átomo propuesto por el químico y físico británico-neozelandés Ernest
Rutherford para explicar los resultados de su "experimento de la lámina de
oro",.
La importancia del modelo de Rutherford no residió en proponer la existencia de un núcleo en el átomo. Término que, paradójicamente, no aparece en sus escritos. Lo que Rutherford consideró esencial, para explicar los resultados experimentales, fue "una concentración de carga" en el centro del átomo, ya que si no, no podía explicarse que algunas partículas fueran rebotadas en dirección casi opuesta a la incidente. Este fue un paso crucial en la comprensión de la materia, ya implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa.
La importancia del modelo de Rutherford no residió en proponer la existencia de un núcleo en el átomo. Término que, paradójicamente, no aparece en sus escritos. Lo que Rutherford consideró esencial, para explicar los resultados experimentales, fue "una concentración de carga" en el centro del átomo, ya que si no, no podía explicarse que algunas partículas fueran rebotadas en dirección casi opuesta a la incidente. Este fue un paso crucial en la comprensión de la materia, ya implicaba la existencia de un núcleo atómico donde se concentraba toda la carga positiva y más del 99,9% de la masa.








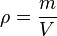
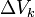 (convergiendo hacia un volumen muy pequeño) y estén centrados alrededor de un punto, siendo
(convergiendo hacia un volumen muy pequeño) y estén centrados alrededor de un punto, siendo  la masa contenida en cada uno de los volúmenes anteriores, la densidad en el punto común a todos esos volúmenes:
la masa contenida en cada uno de los volúmenes anteriores, la densidad en el punto común a todos esos volúmenes: